イオン・pH・mol・mEqなどの用語や単位が出てきます。
これらを理解するには、原子のことを知るのが早道です。
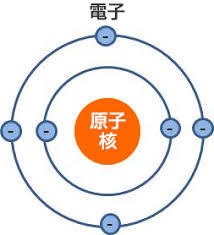
原子は、陽子と中性子から成る原子核と、その周囲を回る電子からできています。
陽子は+電荷を持ち、電子はー電荷を持っており、原子では必ず同じ数です。
水素なら陽子1個と電子1個、酸素なら陽子8個と電子8個です。
右図のように電子が6個だということは、原子核に陽子が6個あることになります。
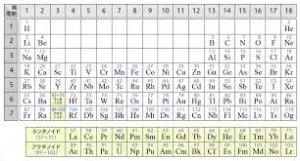
「原子番号」は陽子の数で決まり、陽子6個は原子番号6で、原子名は炭素です。
原子核には陽子の他に中性子もあり、この粒子は電荷を持っていません。
原子核という狭い空間に+電荷を持った陽子が多数あると、電気的な反発で飛び出してしまいますが、中性子がつなぎ役となってまとめています。
原子の重さのことを「原子量」と言い、陽子・中性子・電子の重さを足したものになりますが、陽子と中性子はほぼ同じ重さなのに対して、電子は非常に軽くて1000個あっても陽子1個分の重さもないため、陽子+中性子を原子量としています。
陽子が定数であるのに対して、原子核に入る中性子の数には特に決まりがありません。
原子番号1の水素を例にしますと、原子番号と陽子の数は同じですから、原子核に陽子が1個あるのは確定です。
陽子1個なら電気的な反発がないので、通常の水素は中性子を持っていません。
しかし、中性子を1個持つ重水素や、中性子を2個持つ三重水素というものが極めてわずかですが存在します。
陽子の数は1なので原子番号はどれも1ですが、原子量は水素が1・重水素が2・三重水素が3です。
このように、中性子の数が違うことによって、原子番号は同じだけれども原子量が違うものを同位元素と言います。
理科年表に記載されている水素の原子量は1.0079で、小さな端数があるのは自然界にあるわずかな同位元素のためです。(通常は水素の原子量=1と覚えれば十分です)
原子番号が大きくなるに従って、中性子の数が増えていく傾向があり、原子番号92のウランでは、陽子92個と中性子147個で原子核を作り、原子量は239です。(ちなみに、核分裂するのは中性子が4個少ない原子量235のウランです)
電子に話を移します。
電子は太陽の周りを惑星が巡るように、原子核の周りを回っています。
太陽系の構造と少し違うのは、地球の軌道上には他の惑星がいませんが、原子では同じ軌道を回る電子があることです。
各軌道に入ることができる電子の数に上限があり、最も内側の軌道は2個・2番目の軌道は8個・3番目の軌道も8個・4番目の軌道は18個・・・です。
通常は内側から順に埋まっていきます。
原子番号3のリチウムであれば、陽子3個ですから電子も3個で、最も内側に2個が入り、2番目に1個入ります。
電子配列としては、各軌道が定数通りに埋まった状態が最も安定します。
リチウムでは、最も内側は定数2に対して2個入り、2番目は定数8に対して1個しか入っていませんので、外側の1個を放出した方が電子配列は安定します。
原子番号9のフッ素では、最も内側は定数の2個が入り、2番目は定数8のうち7個まで入りますので、他からか電子を1個借りてくると安定します。(7個を放出することも理論的には可能なのですが、4個以上の貸し借りは通常では起こりません)
電子を放出するということは、-電荷が減ることになり、残りは+電荷を帯びることになります。
これを陽イオンと言い、元素記号の右肩に+を付けて表記します。
電子1個を放出したものが1価陽イオンで右肩に+が付き、電子2個を放出したものが2価陽イオンで右肩に2+が付きます。
逆に、電子を借りてくるということは、-電荷が増えることになり、全体としてー電荷を帯びます。
これを陰イオンと言い、元素記号の右肩にーを付けて表記します。
陽イオンと同じように、電子1個を借りたものが1価陰イオンで右肩にーが付き、2個借りたものが2価陰イオンで右肩に2-が付きます。
電子を放出しやすい原子は陽イオンになりやすく、電子を借りようとする原子は陰イオンになりやすい性質を持つことになります。