DNAがコードするのは20種類の α-L-アミノ酸
自然界には,アミノ酸は500種以上存在する
必須アミノ酸----人は,8種類を合成できないし,2種類は十分な量を合成できない.
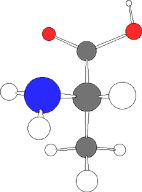 | 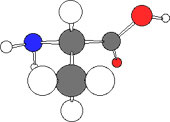 | |||
| 図 8.1 フィッシャーの投影法によるL-アラニン | 図 8.2 アミノ基を左,カルボキシル基を右にしたL-アラニン.メチル基(アルキル基)が手前の下になる |
タンパク質はアミノ酸の重合体であるが,タンパク質のアミノ酸シーケンスは,通常アミノ基のN末端を左に書き,カルボキシル基(C末端)を右に書く.上に水素,下にアルキル基になるが,水素とアルキル基は手前にでている構造になる.
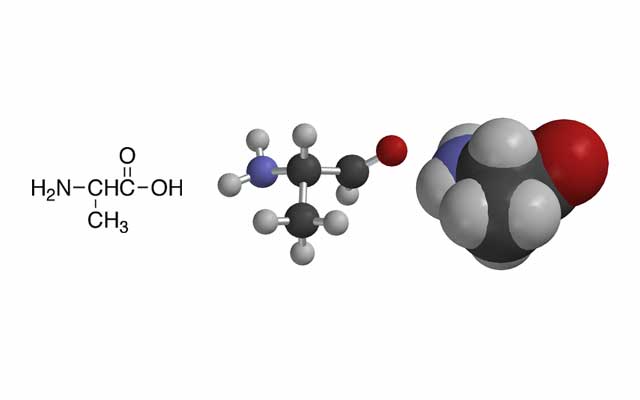
アラニンを示すいくつかのモデル
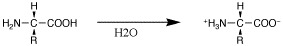
アミノ酸の構造式は,化学系の本では左のように,生物系の本では右のようにそれぞれ書いてある.化学系では固体状態や水溶液では広い範囲のpHを扱う.生体内では,中性付近の水溶液でイオンしている状態を主に扱う.
アミノ酸は水溶液中で,溶液のpHによってイオン化の状態がかわる
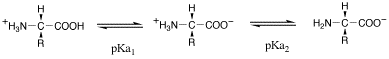
アミノ酸の電離によって生じる正電荷と負電荷の数が等しくなるpHを等電点(pI)と呼ぶ.
等電点は,2つの酸解離指数の平均値で求められる
pKa1 + pKa2
pI =
2
側鎖にカルボキシル基のあるグルタミン酸は,pKaが3つあるアミノ酸
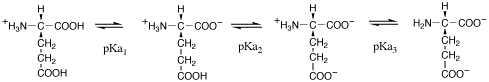
等電点(pI)は,<正電荷と負電荷の数が等しくなる状態の左右の pKaの平均となる.BR>
pKa1 + pKa2
pI =
2
問い
側鎖にアミノ基のあるリシンでは,等電点(pI)は,どうなるか
酸性
中性
アルカリ性
親水性
疎水性
- ニンヒドリン
アミノ酸とニンヒドリンが反応すると紫色に発色する.pH 5ぐらいがよい.
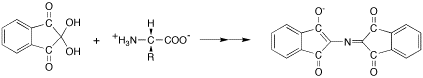
すべてのアミノ酸と反応し,発色する.570 nm での吸収を測定するが,プロリンとヒスチジンは,それぞれ黄色と青色になる.
- タンパク質の分解
タンパク質に濃硫酸と触媒(CuSO4,K2SO4)を加え加熱すると,タンパク質のアミノ酸は,アンモニアまで分解され,硫酸アンモニウムとなる.
溶液を水酸化ナトリウムでアルカリ性とし,遊離するアンモニアを水蒸気蒸留で分離し,既知モル数の硫酸で吸収する.そののち,中和滴定すると全タンパク質として算出できる(ケルダール法) - タンパク質の加水分解
6 M の塩酸溶液に溶解し,酸素除去の後,110℃で24時間加熱すると,タンパク質のアミド結合が加水分解して,アミノ酸に分解する.
ただし,システインとメチオニンは,過ギ酸による酸化の後,加水分解する.
トリプトファンは,水酸化バリウム(あるいはナトリウム)による加水分解
アミノ酸の分析は,液体クロマトグラフ(ポストカラム)が一般的
- タンパク質のN末端からの分解 (シーケンスの分析)
タンパク質のN末端のアミノ基とフェニルイソチオシアネートを反応させた後,限定的分解をして,アミノ酸を一つだけ切り出す.
(エドマン法)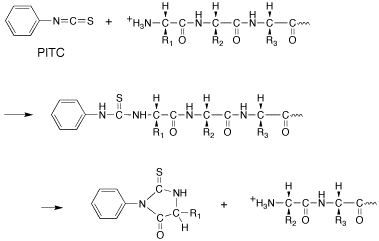
- ペプチド結合(アミド結合)
カルボキシル基とアミノ基で脱水縮合する反応でアミド基
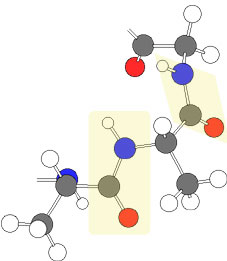
アミド結合部は,回転できなくなるので,タンパク質の立体構造の安定性に寄与する
食品中のアミノ酸組成
制限アミノ酸 基準タンパク質に含まれる必須アミノ酸とくらべて,最も割合の低いアミノ酸
スコアリングパターン
| アミノ酸 | mg/g | |
| イソロイシン | 40 | |
| ロイシン | 70 | |
| リシン | 55 | |
| メチオニン, シスチン | 35 | |
| フェニルアラニン チロシン | 60 | |
| スレオニン | 40 | |
| トリプトファン | 10 | |
| バリン | 50 |