化学反応の反応物と生成物について,ギブスの自由エネルギーの差を調べると,反応がどちらの方向に進むのかわかる.一般的な反応,式 24.1において,そのギブスの自由エネルギーの差が負であれば,反応は,左から右へと進むといえる.しかし,反応が完全に進行するわけではない.つまり,AとBが完全になくなり,CとDだけになることはない.
A + B -> C + D 式 24.1
基本的には,ABCDの4つの物質が存在するところで,反応が止まる.ギブスの自由エネルギーの差が負であることは,AとBよりもCとDが多いところで,反応が停止するということを示してるだけである.この停止した状態が,平衡状態であり,化学平衡と呼ばれる.化学平衡は,やはり,ギブスの自由エネルギーと密接に関係している.
平衡定数
反応,式 24.1において,平衡定数 K が式24.2で定義される.
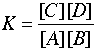 式 24.2
式 24.2
ここで,[A]は,物質Aの物質量である.濃度(厳密には活量)でもよいし,モル数でもよいが,統一していればよい.平衡定数Kは,定数ではあるが,温度には依存している.平衡定数は,化学反応によって定まる量である.平衡定数がわかっていれば,反応を起こされる物質の量によって,どこまで反応が進行し,生成物がどれだけ得られるかを,計算で知ることができる.
平衡状態では,反応容器内の,それぞれの物質についてのギブスの自由エネルギーの合計がもっとも小さくなっている.反応をより単純にして,AとBの平衡について考えてみる.(図24.1)
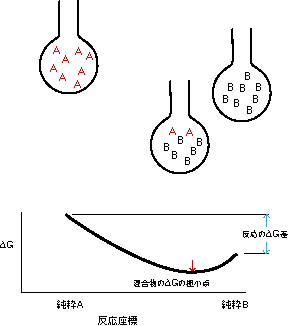
図24.1 反応( A <--> B )についてフラスコ内の様子と自由エネルギーの変化
反応の自由エネルギーの差は,純粋BのDGBから,純粋AのDGAを引いた値である.もともと,DGは,エントロピー項を持っているので,反応の中間状態では,混合によるエントロピーがあり,DGが低下する.そのため,反応は,純粋Bの状態の手前で停止する.この,混合による効果は,反応のDGから求めることができるのである.
物質量の変化とギブス自由エネルギーとの関係(化学ポテンシャル)から,系の自由エネルギーの極小値を求めることで,重要な式, 24.3 が得られる.
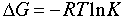 式 24.3
式 24.3
ここで,DGは,純物質についてのギブス自由エネルギーをもとに求めた,反応のギブスの自由エネルギー差である.式に,温度Tが含まれていることに,注意すること.(ただし,DG自身も温度の関数である).式 24.3の左辺は,純物質についてのギブス自由エネルギー差であるが,右辺は,混合物のエントロピー項であることは,おもしろい.式24.3は,指数形に変形すると,
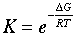 式 24.4
式 24.4
式24.4は,ボルツマン分布の式と形が同じであることに,注目しよう.
化学平衡は,様々なところに現れる.
溶解度積 (溶解度)
銀イオンと塩素イオンの組み合わせでは,塩化銀が沈殿する.
Ag+ + Cl- --> AgCl
この反応においても,すべの反応物がAgClまで進行するのではなく,銀イオンと塩素イオンがわずかであるが残る.つまり,この反応においても,化学平衡が成り立っているのである.塩化銀は固体であるので,濃度の概念はなく,[AgCl] = 1 と置き,溶解度積,Kspが定義される.
Ksp = [Ag+][Cl-] = 1.8 x10-10
つまり,約1.3 x10-5 mol /L 程度の銀イオンと塩素イオンが残っているのである.溶解度積,Kspもまた,自由エネルギーに起因する量である.
酸塩基解離定数