化学反応などの変化について述べているのは,熱力学第2法則である,エントロヒ゜ー増大則である.変化は,全体のエントロピーが増大する方向に起こる.
ノート22において,ギブスの自由エネルギーを導入したが,これは,全体のエントロピーを,系の量に置き換えた関数である.
全体のエントロピーとギブスの自由エネルギーは符号が反対なので,化学反応などの変化は,自由エネルギーの低下する方向に進む.
水素と酸素が反応して,水が生成する,化学反応を例に見てみよう. ( 図 23.1)
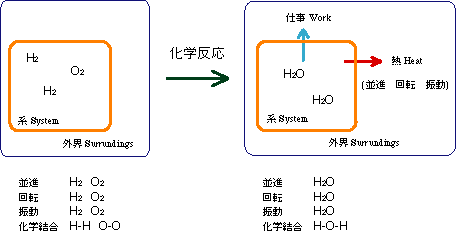
図 23.1 水素と酸素の燃焼による状態の変化
反応の前と後を比較すると,
系と外界の合計のエネルギー,すなわち,全エネルギーは変わっていない.
エネルギーの保持のされている場所が変わっている.
エネルギーの保持のされ方が変わっている.
反応の結果,エネルギーの分布が多様化している.このことは,状態の数の増加であり,全体のエントロピーの増加になっている.
様々な計算に利用できる,標準モルギブス自由エネルギーが定められている.これは,各元素の安定な状態を基準とし,1 気圧で1モルの値を,0 としている.
水素と酸素から水が生成する化学反応について,ギブスの自由エネルギーの変化を求めてみる.ギブスの自由エネルギーの変化は,
ΔG = 生成物のΔGの合計 - 反応物のΔGの合計
反応式は,
2H2 + O2 -> 2H2O
ΔG = (2 x ΔG H2O ) - (2 x ΔG H2 + ΔG O2 )
標準モルギブス自由エネルギーの表から値を調べ,代入する.
ΔG = (2 x -228.6 ) - (2 x 0 + 0 ) = -457.2 kJ/mol
負の値であることから,反応は,自発的に進行することがわかる.この結果は,当たり前のように思うかもしれない.しかし,温度を上げていくと,ΔGの値が,正の値となり,反応の方向が逆になる.