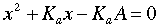
脚注 26
| 物質 | pKa | 物質 | |
| アスコルビン酸(1) | 4.03 | ||
| アラニン(1) | 2.30 | ||
| クエン酸(1) | 2.90 | ||
| クエン酸(2) | 4.34 | ||
| 酢酸 | 4.76 * | ||
| HCN | 9.21 | ||
| 塩酸 | -8 | ||
| H2CO3(1) | 6.35 | ||
| H2CO3(2) | 10.33 |
化学便覧,4th.ed.,丸善,1993
* Handbook of chemistry and physics,80th.ed. CRC Press,2000. !! 化学便覧の値(4.56)はまちがっていると思われる.!!
イオンの濃度が高いときは,その量に見合った効果を発揮しない.活量は,実質的な効果を及ぼす濃度の意味で,活量は,濃度より小さい値である.濃度が希薄になると,活量と濃度は等しいとしてよい.濃度が0.001 mol/L以上では,注意が必要である.活量 a と濃度 C は,活量係数 γ で関係づけられている.
a = γ C
表 26.2 種々の物質の平均活量係数 γ
| 物質 mol/kg -> | 0.001 | 0.01 | 0.1 | 1 | 10 |
| AgNO3 | 0.964 | 0.896 | 0.732 | 0.430 | 0.108 |
| CaCl2 | 0.888 | 0.727 | 0.517 | 0.495 | 43.1 |
| CuCl2 | 0.887 | 0.722 | 0.495 | 0.405 | |
| HCl | 0.965 | 0.905 | 0.797 | 0.811 | 10.4 |
| HF | 0.551 | 0.225 | 0.0766 | 0.0249 | 0.0085 |
| HNO3 | 0.965 | 0.905 | 0.792 | 0.730 | 1.644 |
| KCl | 0.965 | 0.901 | 0.768 | 0.604 | |
| KOH | 0.965 | 0.902 | 0.779 | 0.733 | 6.11 |
| NH4Cl | 0.965 | 0.901 | 0.769 | 0.603 | |
| NaOH | 0.965 | 0.902 | 0.775 | 0.674 | 3.258 |
参考 Handbook of chemistry and physics,74th.ed. CRC Press,1993.
ふつう,水素イオンと言うと,H+ のように書くが,これは疑問である.水素原子から,電子がとれたのが,水素イオンであるが,となると,陽子(プロトン)のことである.陽子が,水の中で安定に存在しているのは,考えにくい(ないことはないのだけれど).それゆえ,水分子のローンペアに陽子がついた状態である,ヒドロニウムイオンとして扱うのがとりあえず適当である.なお,水素イオンのことを,プロトンと言うこともある.
ヒドロニウムイオン H3O+
つぎの2次方程式を解くことになる.
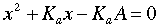
解は,
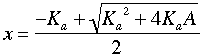 (解は正の値が一つである.)
(解は正の値が一つである.)
この式により,計算する.酢酸のKaは,1.74 x 10 -5であるので,酢酸溶液,1 mol/Lでは,解離している酢酸の量は,5.9 x 10 -3 mol/L 程度となる.近似をした場合の値 4.2 x 10 -3 mol/Lは,この値と比べてそんなに離れていない.
残念ながら,実際は,様々な効果があるため,この式でもまだ正確ではない.
-----------------
なを,2次方程式の根の公式は,
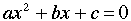 に対して,
に対して,
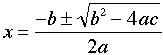 である.
である.
厳密にいえば,水素イオンの活量であるが,とりあえず,濃度でよい.
| 戻る | 化学質問箱 | 目次ページ | Copyright 2001-2002, Y.Naka. Last updated, Sep .18, 2002. |