脚注 8
結合性軌道と反結合性軌道は,原子軌道を基に,分子の軌道を表現するのに使われる.本来は,その分子を構成するすべての原子核と電子に対して,波動方程式を解くことで,分子の軌道を求めるべきである.ただし,これは不可能である.また,原子軌道をもとにした説明でも,現実を十分説明できる.より,理論に近い方法もあるが,これはさらに勉強しなければならない.化学を専門にしない学生の場合は,こういった事情を知っていれば,十分である.
s軌道とs*軌道の積の空間積分は0になり,2つの軌道は直交している.
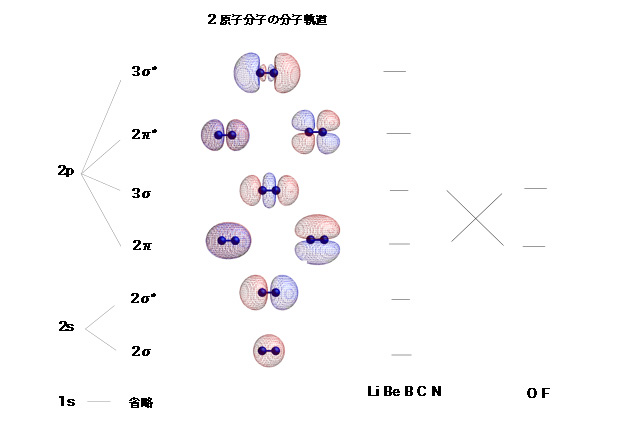
化学結合を考えるとき,軌道や結合の対称性は重要である. 原子軌道の重なりによって,化学結合を考えるとき,原子軌道の重なり方によって,結合の種類を分類している.
| 戻る | 化学質問箱 | 目次ページ | Copyright 2001-2004, Y.Naka. Updated, June 20, 2004. |