エネルギー準位
水素原子の場合のように,軌道電子が1つしかない場合には,エネルギー準位は,そろっている.しかし,電子の数が増えると,電子同士の反発が軌道のエネルギー準位に影響する.原子核に近い軌道に存在する電子は,核の陽電荷を少し遮蔽する効果があり,外殻の軌道のエネルギー準位は高くなる.また,s軌道の電子は,p軌道の電子よりも,内側に存在する確率が大きいので,p 軌道のエネルギー準位は,s 軌道のエネルギー準位よりも高くなる.同様に,d 軌道のエネルギー準位は,p 軌道のエネルギー準位よりも高くなる.

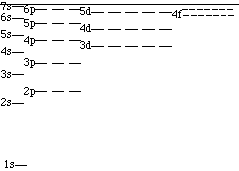
図 水素原子(左) と その他の原子(右) のエネルギー準位図
パウリの排他原理
一つの軌道には,スピンを異にして,電子は2つまで入ることができる.
原理とは,絶対的な規則である.一つの軌道に電子が3つ入ることはありえない.
本来は,電子は同じ状態をとれないということである.電子の状態を記述する n,l,m,s 量子がすべてことなるということである.スピンを異にするということで,1つの軌道には電子は,2つはいることになる.
縮退している複数の軌道に電子が入るときは,まず,異なる軌道に分散する.
フントの規則は,絶対的ではない.
電子配置
パウリの排他原理とフントの規則に従って,エネルギー準位の低いところから,順番に入っていく.周期率表と比べながら,電子配置を考えてみなさい.
ナトリウムは原子番号 11 であるから,陽子が11 個ある.電気的に中性のナトリウム原子では,電子は, 11 個存在する.上に示した規則に従って,11 個の電子を配置した様子を示す.
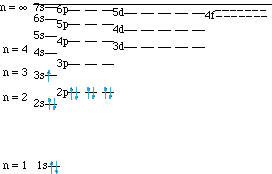
図 ナトリウム原子の電子配置
魚を焼いたとき,炎が時々,オレンジ色になるでしょう.あるいは,高速道路のトンネルの照明は,オレンジ色でしょう.これらのオレンジ色の光は,ナトリウムの原子スペクトルです.ナトリウムの3p-3s間の電子遷移による,発光で,その波長は,589 nmです.
花火の色は,原子スペクトルそのものである.
赤 リチウム
橙 カルシウム
緑 バリウム
青 銅
紫 カリウム