嫟柭岠壥偵傛偭偰兛悈慺傛傝傓偟傠兞悈慺偺傎偆偑揹棧偟傗偡偄丅
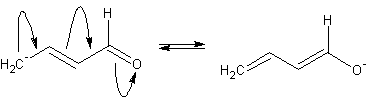
偡傞偲丄弅崌屻僸僪儘僉僔儖婎偼兟扽慺偵偮偔丅
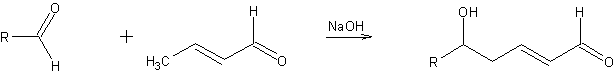
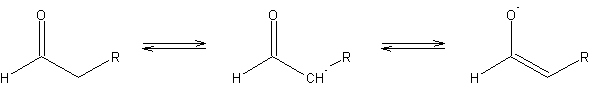
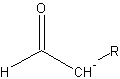
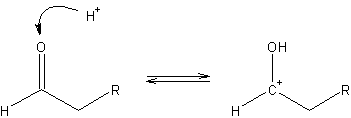
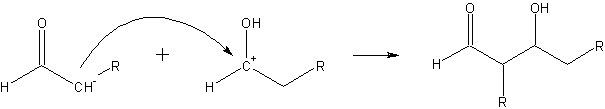
傕偆堦偮丅僋儘僩儞傾儖僨僸僪偺傛偆側價僯儖婎偵傾儖僨僸僪婎偑晅偄偰偄傞傛偆側傕偺偼丄
嫟柭岠壥偵傛偭偰兛悈慺傛傝傓偟傠兞悈慺偺傎偆偑揹棧偟傗偡偄丅
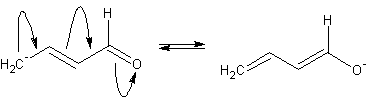
偡傞偲丄弅崌屻僸僪儘僉僔儖婎偼兟扽慺偵偮偔丅
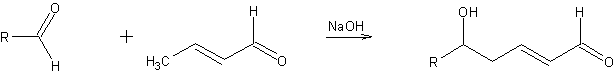
| 傾儖僨僸僪 | R-CHO |
| 傾儖僪乕儖 | 傾儖僪乮傾儖僨僸僪乯亄僆乕儖乮傾儖僐乕儖乯丅懡暘 |
| 兛丄兝扽慺 | 僇儖儃僯儖婎偑偁傞偲偒偺扽慺偺埵抲偺昞偟曽丅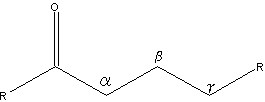 |
| 僇儖儃僯儖婎 | C=O偺擇廳寢崌 |
| pKa | 巁揹棧掕悢丅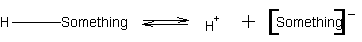 偲偐尵偆暯峵忬懺偵偁傞偲偒丄 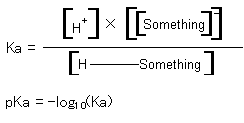 偱掕傑傞掕悢 椺偊偽丄pKa偑侾侽彫偝偔側傞偲丄 H+偑10000000000攞揹棧偟傗偡偔側傞丅 |
| 僇儖儃傾僯僆儞丒僇僠僆儞 | 桳婡偱斀墳拞娫懱傪峫偊傞帪偵廳梫丅 峔憿幃傪彂偄偰丄偁傞扽慺偐傜扨寢崌偺榬偑俁杮偟偐怢傃偰偄側偄偲偒丄 偦偺扽慺偺揹巕懳傪悢偊偰傒偰丄 3屄偺偲偒乧偦偺扽慺尨巕偼亄偺揹壸傪懷傃傞丅揹巕偑俇偮偟偐側偄丅 亄側扽暘巕傪僇儖儃僇僠僆儞偲偄偆丅 4屄偺偲偒乧偦偺扽慺尨巕偼亅偺揹壸傪懷傃傞丅旕嫟桳揹巕懳傕帩偮丅 亅側扽暘巕傪僇儖儃傾僯僆儞偲偄偆丅 |
| 儀儞僘傾儖僨僸僪 benzaldehyde | 傾儖僨僸僪偺堦庬丅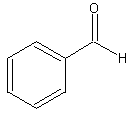 |
| 僋儘僩儞傾儖僨僸僪 | 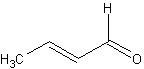 |