侾丏奣梫
悈慺偲巁慺傪懱愊斾俀丗侾偱崿偤偁傢偣偰揰壩偡傞偲敋敪揑偵壔崌偟丆偦偺戝偒側壒偵嬃偐偝傟傑偡丅儐乕僕僆儊乕僞偼丆偙偺偨傔偺幚尡憰抲偲偟偰傛偔抦傜傟丆奺庬偺庤嶌傝昳傕妶桇偟偰偄傑偡丅偟偐偟丆偙傟傜偼抲姺暔幙偲偟偰悈傪梡偄偨傕偺偑戝敿偱丆壔崌偟偰弌棃偨悈偺妋擣偑偱偒傑偣傫丅偦偙偱丆姡偄偨帋尡娗偵擖傟偨悈慺偵揰壩偟偰偱偒傞悈揌傪妋擣偟偨傝丆悈慺偺墛傪崟斅偵摉偰偰偱偒傞悈揌偱奊傪昤偄偨傝偡傞墘帵幚尡偑岺晇偝傟偰偒傑偟偨丅偟偐偟丆奐曻宯偱擱偊偰悈偑偱偒傞偺偼晛捠偺尰徾偱偁傝丆廫暘側徹柧幚尡偲偼偄偊傑偣傫丅
偦偙偱丆擱偊偰偱偒傞悈揌傪妋擣偱偒傞暵嵔宯偺婍嬶傪専摙偟偰偄傞偲偒丆偍傕偟傠偄傕偺傪巚偄弌偟傑偟偨丅挿偄價僯儖僠儏乕僽偵悈慺偲巁慺傪枮偨偟偰曅抂偵揰壩偡傞偲僠儏乕僽撪傪墛偑憱傝丆悈揌偱敀偔撥傞偲偄偆傕偺偱偡丅怴嵦偺崰丆摨椈偺愭惗偐傜暦偄偨幚尡偱丆峀偔幚慔偝傟偰偄傞傕偺偩偲巚偄崬傫偱偄傑偟偨丅偲偙傠偑丆庢傝慻傒巒傔偨1990擭摉帪偼丆帒椏傗巗斕昳側偳傪尒偮偗傞帠偑弌棃傑偣傫丅巇曽側偔丆埲壓偺傛偆側峔憿傪峫偊偰攝晍偟偨偲偙傠昡敾偵側傞偲偲傕偵丆巚偄偮偒偺柤徧偱偁傞乽壩偺嬍僟僢僔儏乿偑堦斒壔偡傞傛偆偵側傝傑偟偨丅傑偨丆偙偺幚尡偼丆偨偔偝傫偺惗搆偑庤尦偱摨帪偵懱尡偱偒傞報徾怺偄傕偺偱偁傝丆乽僷僗僇儖揹慄乿偺壔妛斉偵偟偨偄偲偄偆栚榑尒傕偁傝傑偟偨丅
乽壩偺嬍僟僢僔儏乿偺摿挜
嘆悈偺揹婥暘夝偵傛傝敪惗偟偨悈慺偲巁慺偺棙梡
乮悈仺揹婥暘夝仺婥懱仺揰壩仺悈乯偺堦楢偺夁掱偑戝愗偩偲峫偊丆乽揹婥暘夝憛乿偺懚嵼傪慜採偵偟傑偟偨丅廬偭偰丆悈慺儃儞儀偲巁慺儃儞儀偐傜摫偄偨婥懱偺棙梡偼丆堄恾揑偵旔偗傑偟偨丅
嘇乽揹婥暘夝憛乿偲乽揰壩摏乿偺暘棧峔憿
婍嬶偼丆乽揹婥暘夝憛乶偲丆埑揹慺巕偵傛傞壩壴偱崿崌婥懱偵揰壩偡傞乵揰壩摏乶偐傜偱偒偰偄傑偡丅偙偺椉幰傪愗傝棧偟偰偐傜揰壩偡傞傛偆偵偟偨偨傔丆乽揹婥暘夝憛乿撪傊壩偑擖偭偰敋敪偡傞帠屘傪杊偘傑偡丅傑偨丆愗傝棧偟晹暘偵僑儉僉儍僢僾偺僷僢僉儞傪巊梡偟偨偨傔乵揰壩摏乶撪傊偺嬻婥偺崿擖偑側偔丆揰壩偑妋幚偵側傝傑偡丅
拲丗椉幰偺愗傝棧偟傪朰傟偰揰壩偡傞偲丆乽揹婥暘夝憛乿撪偱偺敋敪偺婋尟偑偁傝傑偡丅偦偙偱丆乽揹婥暘夝憛乿撪偺嬻娫傪嬌椡彫偝偔偟偰戝偒側敋敪傪杊偓傑偟偨丅傑偨丆乽揰壩摏乿偑攋楐偡傞婋尟偵偮偄偰傕摨條偱丆撪梕愊傪嬌椡彫偝偔偟偰偄傑偡丅
丂 |
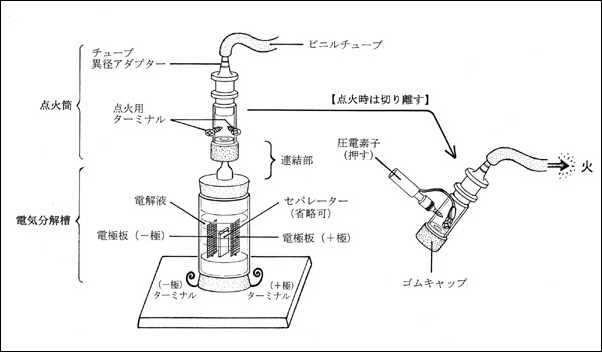
恾侾 乽壩偺嬍僟僢僔儏乿偺奣棯恾
|
俀丏巊梡朄
佱弨旛佲
(1)價僯儖僠儏乕僽偺弨旛
撪宎係mm丆挿偝10乣20倣偺價僯儖僠儏乕僽傪梡偄丆抂傪乽揰壩摏乿偺乽僠儏乕僽堎宎傾僟僾僞乕乿偵憓偟崬傓丅傕偆堦曽偺抂偼丆婋尟杊巭偺偨傔憢偺奜偵弌偡乮壩婥尩嬛乯丅
仸撪宎係mm偼丆婥懱偑棴傑傞帪娫丆悈揌偺妋擣丆埨慡惈側偳傪峫椂偟偨戝偒偝偱偁傞丅
(2)乽揹婥暘夝憛乿偲乽揰壩摏乿偺楢寢
乽揰壩摏乿偺抂偺旐偣偰偁傞惵怓乽僑儉僉儍僢僾乿拞墰偵捾梜巬偱寠傪奐偗丆乽揹婥暘夝憛乿偺僈儔僗僗億僀僩偵嵎偟崬傒丆椉幰傪楢寢偡傞丅
(3)揹婥暘夝
乽揹婥暘夝憛乿偺巜昗埵抲傑偱揹夝塼乮埲壓偺椺嶲徠乯傪擖傟丆侾俙慜屻偺揹棳傪棳偡丅揹棳偼師戞偵憹偊傞偺偱丆弶婜偼侾俙埲壓偲偡傞丅揹棳偑懡偡偓傞偲丆傾儚棫偭偰乽揰壩摏乿撪偵揹夝塼偑擖傝崬傫偩傝丆揹夝塼壏偑崅偔側傝夁偓傞丅
仸揹夝塼偺椺
嘆 NaOH悈梟塼偺椺侾丗 俀亾乮 栺0.5mol/l 乯側傜 4.5倁掱搙
嘇 NaOH悈梟塼偺椺俀丗 侾亾乮 栺0.25mol/l 乯側傜 俇倁掱搙
嘊 Na2CO3悈梟塼偺椺丗 俆亾乮 栺0.5mol/l 乯側傜 俇倁掱搙
嘋 NaHCO3悈梟塼偺椺丗 朞榓悈梟塼乮 栺俋亾丆20亷 乯側傜 俇倁掱搙
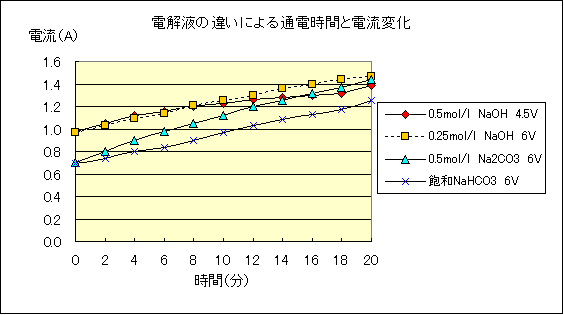
恾俀 揹夝塼偺堘偄偵傛傞捠揹帪娫偲揹棳曄壔
丂 |

恾俁 乽揹尮憰抲乿丆乽壩偺嬍僟僢僔儏乿杮懱丆乽價僯儖僠儏乕僽乿
|
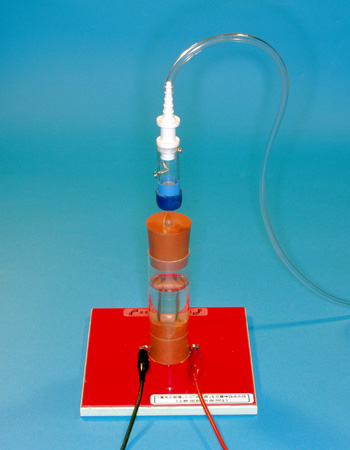
恾係 乽壩偺嬍僟僢僔儏乿杮懱晹暘
|
佱幚尡佲
(1)乽揹婥暘夝憛乿偐傜乽揰壩摏乿傪暘棧屻偵揰壩
婋尟杊巭偺偨傔丆乽揹婥暘夝憛乿偐傜乽揰壩摏乿傪暘棧偟偨屻丆乽揰壩摏乿傪庤偺傂傜偱曪傓傛偆偵偟偰曐帩偟丆埑揹慺巕偺乽揰壩婍乿偱揰壩偡傞乮傾僋儕儖僷僀僾偺攋懝偺晄埨偑懡彮偁傞偺偱丆孯庤傪拝梡偟偨傎偆偑傛偄乯丅
"僷儞"偲偄偆戝偒側壒偲偲傕偵壩偺嬍偑惗搆偺庤尦傪憱傞丅晹壆傪埫偔偟偰偍偔偲丆壩偑傛偔尒偊傞丅幚尡屻偼丆惗惉偟偨悈揌偱價僯儖僠儏乕僽撪偑敀偔撥傞丅
(2)捠揹帪娫
忋婰偺嘆乣嘋偺椺偱20暘娫捠揹偟偨寢壥丆偄偢傟傕悈揌偵傛傞撥傝偑栺俉倣偱偒偨丅廬偭偰丆30暘傕偁傟偽撪宎係mm價僯儖僠儏乕僽栺10倣偺挿偝傑偱崿崌婥懱偑棴傑傞偲峫偊傜傟傞丅
仸偙偺傛偆側梊旛幚尡傪峴偭偰丆悈揌偵傛傞撥傝偺偱偒傞挿偝傪挷傋傞偲悈揌偱枮偨偝傟傞帪娫傪梊憐偱偒傞丅
偨偩丆妛廗偲偟偰偼丆價僯儖僠儏乕僽偺搑拞傑偱悈揌偑偱偒偨曽偑嫽枴怺偄偲巚傢傟傞丅
仸棟榑揑側敪惗検
1A亊20暘亊60昩亖1200俠乮僋乕儘儞乯丂1200俠/96500俠亖0.0124摉検
亄嬌乮巁慺乯丗5600cm3亊0.0124亖栺69cm3
亅嬌乮悈慺乯丗11200cm3亊0.0124亖栺139cm3
崌寁偺婥懱敪惗検亖栺208cm3
價僯儖僠儏乕僽偺抐柺愊丗0.2亊0.2亊3.14亖0.126cm2
208cm3/0.126cm2亖1650cm亖栺16倣
乮寢壥丆幚尡抣偼棟榑抣偺栺1/2検偲側偭偨丅乯
丂 |
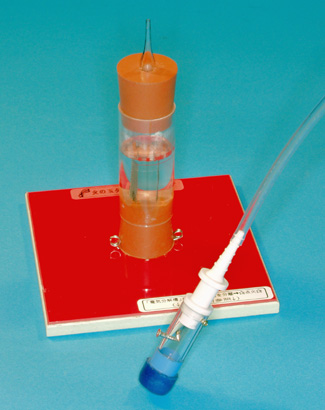
恾俆 乽揹婥暘夝憛乿偲乽揰壩摏乿偺愗傝棧偟
|

恾俇 乽揰壩婍乿傪梡偄偨揰壩
|
佱屻巒枛佲
(1)價僯儖僠儏乕僽撪偺悈揌偺彍嫀
僄傾乕億儞僾偱憲晽偡傞偲栚偵尒偊傞悈揌偼悢暘偱側偔側傞偑丆偝傜偵悢廫暘捠婥偟偰傎偟偄丅
(2)乽揰壩摏乿偺愻忩
惵怓乽僑儉僉儍僢僾乿偲偲傕偵昁梫側傜乽僔儕僐儞僑儉愷乿傕奜偟丆撪晹傪悈愻偡傞丅
乮揹嬌偼僗僥儞儗僗惢側偺偱丆嶬偺怱攝偼側偄丅乯
(3)乽揹婥暘夝憛乿偺愻忩
傾儖僇儕惈偺揹夝塼偱乽僑儉愷乿偑塭嬁傪庴偗傞丅幚尡屻偼丆偡偖偵乽億儕僇乕儃僱僀僩僷僀僾乿傪奜偟丆愻忩偡傞丅
丂乮揹嬌偲揹慄偼僗僥儞儗僗惢側偺偱丆嶬偺怱攝偼側偄丅乯
仸乽揹婥暘夝憛乿偵乽揰壩摏乿傪憓偟崬傫偩傑傑曐懚偟側偄丅
丂 |
僄傾乕億儞僾偱偺悈揌彍嫀仺
傾僋傾傾儕僂儉梡偺僄傾乕億儞僾偺悂偒弌偟岥偲
捈宎係mm偺價僯儖僠儏乕僽偼僒僀僘偑堦抳偡傞丅
|

恾俈 悈揌偺彍嫀
|
俁丏旛峫
丒乽壩偺嬍僟僢僔儏乿偼丆1990擭崰偵尨宆傪嶌惉偟丆嬑柋愭偺尋媶島嵗偵偰幚暔傪攝晍偟偨丅偦偺屻丆奺抧偺尋媶夛偱偺攝晍偲幚墘傪峴偄岲昡偩偭偨偨傔乽慡擔杮嫵怑堳敪柧揥乿偵墳曞偟丆暯惉係擭搙乮1994擭乯偺乽彠椼徿乿傪庴徿偟偨丅偙傟偑丆惓幃側曬崘戞堦崋偱偁傞丅偦偺屻丆1996擭搙偺乽嫗搒巗惵彮擭壢妛僙儞僞乕曬崘VOL.27丆嫗搒巗嫵堢埾堳夛乿偵傕宖嵹偟偨丅
丒偙傟傜傪偒偭偐偗偵慡崙偐傜懡偔偺栤偄崌傢偣傗僥儗價傊偺弌墘埶棅側偳偑憡師偓丆尒杮憲晅側偳偺懳墳傪懕偗偨丅偨偩丆偙偺峔憿偱偺暋惢偺惢嶌偼梕堈偱側偐偭偨偙偲丆揹婥暘夝偱偺婥懱偺敪惗偵帪娫偑偐傞偙偲側偳偵傛傝丆巗斕偺巁慺偲悈慺儃儞儀傪梡偄偨僀儀儞僩偱偺棙梡偑峀偑偭偨丅偙傟偵偮偄偰偼丆巹偺僆儕僕僫儖偲偼偄偊偢丆乽壩偺嬍僟僢僔儏偱偼側偄乿偲偄偆尒夝傪揱偊偨丅側偍丆乽慡擔杮嫵怑堳敪柧揥乿偺怽惪彂椶偵傕丆價僯儖僠儏乕僽撪偱偺斀墳偵娭偟偰偼悪尨偺僆儕僕僫儖偱偼側偄偙偲傪柧婰偟偰偁傞丅
丒乽壩偺嬍僟僢僔儏乿偺巗斕偵岦偗偰奐敪傪恑傔偨嫵嵽夛幮傕偁傞偑丆拞抐偟偰偄傞丅
|







