脚注 13
グラファイトとダイヤモンドは,ともに炭素である(化学式はどちらも, Cn ).しかし,グラファイトとダイヤモンドは,性質が著しくことなる.グラファイトは真っ黒の物質で光を透過せず,電気をよく伝える.一方,ダイヤモンドは透明の物質で,電気を通さない. ダイヤモンドを構成する炭素原子の軌道は,sp3 混成軌道に帰属でき,炭素と炭素の結合は,s結合である.グラファイトを構成する炭素原子の軌道は,sp2 混成軌道に帰属でき,炭素と炭素の結合は,骨格部分はs結合であるが,p 軌道により,p結合も存在する.
炭素原子同士のs結合は,2つの炭素原子のあいだに,結合性軌道と反結合性軌道ができ,結合性軌道に電子が2こ入ることで,エネルギー的に安定化した,強固な結合である.同じ炭素原子の結合でも,p結合は,結合性軌道に電子が2こ入る点では,s結合と同じであるが,広がりが大きく,隣り合う原子にp軌道があれば,共鳴する.ポリエンのように,p結合がつらなる分子では,分子全体にわたって共鳴し,p 軌道の電子は,分子全体を移動することができるようになる.また,ポリエンでは,共鳴するp結合の数がふえることにしたがって,電子の入っている軌道と上位の軌道のエネルギー差が小さくなっている.
 |
||
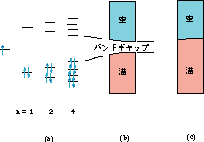
| 図 r12.1 (a)ポリエンでの吸収波長が長くなる様子.(b)きわめて多数の軌道により,エネルギーの帯が形成される様子. b は,半導体の場合.(c)金属の場合. |
 |
||
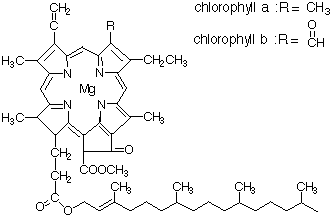
| 図 r12.2 クロロフィルa およびクロロフィルb .ポルフィリン環によって,マグネシウムが固定されている. |
| 戻る | 化学質問箱 | 目次ページ | Copyright 2001, Y.Naka. Updated, 6.25, 2001. |