極めて特殊なケースについて検証してみる.粒子の数が5つの場合である.エネルギー準位は,量子化されており,その間隔は,1 である.その粒子の数が5つの系に,エネルギーがない場合と,大きさ1から4までのエネルギーが保たれている場合について,可能な状態の数を求める.図 20.1 は,エネルギーの大きさが,0の場合と,2の場合について示してある.
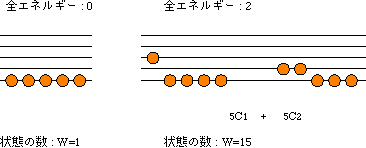
図 20.1 エネルギーと状態数
表 エネルギーの流入と状態数の変化
| 全エネルギー E | 0 | 1 | 2 | 3 | 4 |
| 状態の数 W | 1 | 5 | 15 | 35 | 70 |
| エントロピー S | 小 (0) | 中 | 大 | ||
| 温度 T | 低 (0) | 中 | 高 |
状態の数(W)とエントロヒ゜ー(S)の関係は,
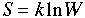 式21.1
式21.1
で定義される.ここで,kは,ボルツマン定数であり,気体定数をアボガドロ数で割った値である.われわれの現実世界では,粒子の数は多い.たとえば,1 molでは,1023もあり,状態の数は,べらぼうな大きさになる.対数をとることによって,扱いやすい大きさの量になる.また,対数をとることによって,可成性となる.すなわち,物質量が増えた場合,状態の数は,かけ算であるが,エントロピーは,足し算である.
熱,温度,エントロピーの関係
(エネルギーがなくてもあっても,)状態の数が1つしかない場合,温度は0である.そこに,エネルギー(熱)が流入してくると,可能な状態の数が増加していく.状態の数の増加は,エントロヒ゜ーの増加である.また,エネルギー(熱)が流入してくるので,温度が上昇する.
温度とは,可能な状態の数の多さと見ることができる.
エントロヒ゜ーの変化は,流入するエネルギーの変化とそのときの温度で表される.系が体積変化などの仕事をしないときは,流入するエネルギーは熱 q であり,エントロピーの変化量は,
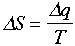 式21.2
式21.2
と定義される.両辺にTをかけると,エネルギーのディメンジョンになることに注意すること.エントロピーの2つの定義(式21.1,式21.2)は,ミクロ的な定義とマクロ的な定義と言え,どちらも正しい.
熱力学の3法則
-
第1法則 エネルギー保存則
-
第2法則 エントロヒ゜ー増大則 変化の本質
-
第3法則 エントロヒ゜ーの基準 絶対0度で,エントロヒ゜ー 0
図 20.2 は,蓄えられているエネルギーは同じであるが,状態数が異なる2つの状態, A と B を表現している.全エネルギーは同じであるので,A と B の間での変化では,エネルギーの増減はない.状態Aでの,W=15は,85回観測したら,15回は,状態Aを観測することを意味する.また同様に,85回観測したら,70回は,状態Bが観測される.可能な状態の数85において,ひとつひとつの可能性は同じである.
2つの状態, A と Bは,同一の物質が,2つの構造をとることができると解釈しよう.2つの構造(すなわち,2つの状態)は,全エネルギーは等しいが,エネルギーの保持の仕方に違いがあり,可能な状態の数がことなるのである.
初めに,一方の状態Aだけを作り出せるとする.この場合は,我々には,注目する物質は,Aとしか見えない.何らかの刺激で,状態Aと状態Bの相互の変化が可能になると,我々には,AかBかのいずれかが観測されるようになる.先に述べたように,確率的には,Bを観測する方が多い.従って,我々は,物質がAからBに変化したように見える.
A と Bの状態は, エントロピーで言うと,Bの方が大きい.すなわち,我々には,AからBに変化において,エントロピーが増大したことになる.
エントロピー増大則は,化学反応などの変化が,確率的に見いだしやすい状態に変化してるだけであることを示している.
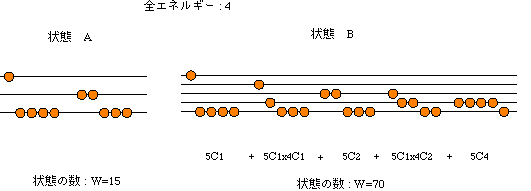
図 20.2 状態の変化 2つの状態のエネルギー準位間隔は,状態Aは2,状態Bは1である.
ボルツマン分布
図 20.2の状態Bを使って説明する.状態Bを70回観測した場合について,各エネルギー準位に見いだす粒子の数を求めてみる.粒子の数は,5つであるが,状態Bを70回観測しているので,粒子の数は,のぺ350個である.これら350個の粒子が,どのエネルギー準位にどれだけの数存在するかを,求める.
e=4 1 x 5C1 = 5
e=3 1 x 5C1 x 4C1 = 20
e=2 2 x 5C2 + 1 x 5C1 x 4C2 = 50
e=1 1 x 5C1 x 4C1 + 2 x 5C1 x 4C2 + 4 x 5C4 = 100
e=0 4 x 5C1 + 3 x 5C1 x 4C1 + 3 x 5C2 + 2 x 5C1 x 4C2+ 1 x 5C4= 175
エネルギー準位の高いところに存在する粒子の数は少なく,エネルギー準位の低いところに存在する粒子の数は多いことがわかる.実際の我々の扱う量のように,粒子の数が多くなると,準位間のエネルギー差と粒子数の分布は,指数関数に従いなめらかな関数になる.これは,ボルツマン分布と呼ばれる.