
| �o�b�e���[�̒m���@�i�Ёj�d�r�H�Ɖ�@������� | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@�P�D�o�b�e���[�̍\���@ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1.1�@�o�b�e���[�Ƃ́E�E�E | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | �@�~�d�r�i�o�b�e���[�j�Ƃ͂Q��ނ̂��ƂȂ����d�ɂƓd���t�Ȃǂ���\������Ă���A���̎����Ă��鉻�w�I�G�l���M�[���A�d�C�I�G�l���M�[�Ƃ��Ď��o�����Ƃ��ł��A�܂��t�ɊO������d�C�I�G�l���M�[��^����ƁA���̌`�̉��w�I�G�l���M�[�Ƃ��Ē~���邱�Ƃ��ł��鑕�u�ł���B |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
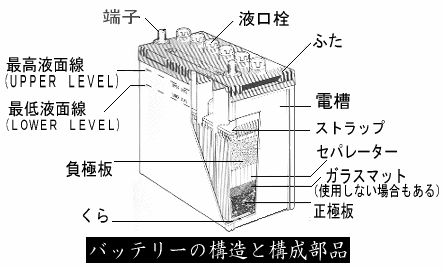
| 1.2�@�o�b�e���[�̍\�� | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | �@�o�b�e���[�ɂ͍\�����̑���ɂ���āA��X�̎�ނ����邪�A�����ԗp�o�b�e���[�ɂ̓y�[�X�g�����o�b�e���[���g�p����Ă���B�����ԗp�o�b�e���[�̏d�v�Ȗ����́A�G���W���n�����̃X�^�[�^�ɓd�͂��������邱�Ƃł���B�G���W����]���ɂ͔��d�@�i�I���^�l�[�^�[�j�ɂ���Ē�d���œd�͂���������o�b�e���[����d���ŕ����[�d�����V�X�e���ɂȂ��Ă���B | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | �@���ɔ���ѕ��ɔ͏�}�Ɏ����悤�ȉ��������i�q�̋�ԂɁA������_�������_�ŗ����č�����y�[�X�g���[�ĂāA�����A�����Ȃǂ̍H�����o�āA���ɔ͓�_�����A���ɔ͊C�ȏ��������Ƃ������̂ł���B�i�q�͊�������ێ����āA�E����h�~���邱�ƂƁA�O���Ɗ������̊Ԃ̓d�C�`���̖�ڂ��͂������̂ŁA�@�B�I���x������A���_�ɑ���ϐH�����傫���A���d�����̂悢���Ƃ��K�v�ł���B ��ʂɊi�q�̓A���`�����܂��̓J���V�E���Ȃǂ�Y�������������ł���A�Y�������͉����ł��A�������A���i�q�̐�����e�Ղɂ��邽�߂ɗp������B���ɔ̊������ł����_�����́A�������F�̌����������q�W���̂ŁA���E���ɕx�݁A���q�Ԃ�d���t�̊g�U�Z�������R�ɂł���悤�ɐ�������Ă��邱�̊������͗��q�Ԃ̌����͂���r�I�R�����̂ŁA�g�p�N���̌o�߂ɂ�āA���������q���j��Ĕ������A�Ō�ɂ͋ɔ���E�����āA�o�b�e���[�̎��������錴���ƂȂ邱�Ƃ������B ���ɔ̊������ł���C�ȏ́A�D�F�ő��E���Ɣ������ɕx�����͂��������߁A���ɔ̓�_�����̂悤�ȒE���͏��Ȃ����A�g�p�N���������Ȃ�ƁA�������������ċɔ̑��E�x�����������A���������邱�Ƃ������B�����h�~���邽�߂ɁA�c���܂��������ɓY�����A�����̉������͂����Ă���B�Z�p���[�^�[�i�u���j�͐��ɔƕ��ɔ̊Ԃɑ}�����ꗼ�ɔ̃V���[�g�i�Z���j��h�~���邽�߂Ɏg�p�����B���ɔ��V���[�g����A�o�b�e���[�͒~�����d�C�I�G�l���M�[��Z���ԂɎ����A�d�������o�����Ƃ��ł��Ȃ��Ȃ�B |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | �@�Z�p���[�^�̕K�v�����́A��d�����ő��E���ɕx�݁A�d���t�̊g�U�����R�ɍs���i�d�C��R���Ⴍ�j�A�@�B�I�ɂ���v�Ŏ_�ɂ��ς��A�ɔɈ��e��������ڂ��悤�ȕ�����n�o���Ȃ����Ƃł���B���̂悤�ȏ�����������̂Ƃ��āA���������Z�p���[�^���g�p����Ă���B�Z�p���[�^�ɂ͕���̂��́A��̂��̂Ȃǂ�����B�����̃Z�p���[�^�́A�K���X�}�b�g�p���Ďg���ꍇ�ƁA�K���X�}�b�g���g�p���Ȃ��ꍇ�Ƃ�����B�K���X�}�b�g�͔��ɍׂ��K���X�@�ۂ��c���Ɍ��������t�F���g��ɂ������̂ŁA����𐳋ɔƃZ�p���[�^�̊Ԃɔz�����ɔ��������邱�Ƃɂ��A�������̒E����h�~�����ڂ�����B | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | �@�ɔQ�͐��ɔA���ɔ���уZ�p���[�^�̕K�v�Ȗ������d�ˍ��킹�A�ɒ��t�X�g���b�v�ɗn�ڂ������̂ł���B�Z���i�P�d�r�j�͂P�̋ɔQ���\�����ꂽ�o�b�e���[�ŁA���̊J�H�d���͋ɔ̑傫���▇���ɊW�Ȃ��A��@2.1V�ł���B�����ԗp�̂P�Q�u�o�b�e���[�́A�Z�����U����ɐڑ����Ă���B �d���͍��������ŏ�}�̂悤�Ɉ�̂ɐ��^����A�P�Q�u�o�b�e���[�ł͘Z�̃Z���ɋ�悳��Ă���B��ʂɓd���̊e�Z���ꕔ�ɂ́u����v������A���ɔA���ɔ̑������ʁX�́u����v�ɏ��悤�ɂȂ��Ă���B����̖�ڂ͋ɔQ���x����ƂƂ��ɁA�ɔ���E�������������̒��a�A�͐ςɂ��V���[�g��h�~���邱�Ƃł���B�ӂ��͎�Ƃ��č��������̈ꖇ�Ԃ��ŁA�ڒ��܂܂��͗n���ɂ��d���̊��S�ɐڒ������A�@����ۂ悤�ɂ��Ă���B���̂ӂ��ɂ́A�_�A�������̒������邢�͓d���t�̖��x�i��d�j���P�A���x�̌v���̂��߂̉t��������B���̉t������d���t���R�ꂽ��A���݂�����Ȃ��悤�ɍ��������̉t���������Ă���B���̐��̏㕔�܂��͑����ɂ͔r�C�E�i�E�j������A�o�b�e���[�������甭�����鐅�f�K�X����ю_�f�K�X����o����悤�ɂȂ��Ă���B |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | ���P�F�d���t�̖��x���w��d�x�Ƃ��ĂԂ��A�������͖��x�ł���B�������]������o�b�e���[�Ɋւ��Ă͔�d�Ƃ����Ăѕ�����ʓI�ł���A����Ղ����߁A�����ł͈ȉ��A�w��d�x�ƌ����B | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@�@ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | �@�e�Z���͉������Œ���ɐڑ�����Ă���B�ڍ����̑����́A�傫�ȃG���W���n���d��������Ă��A�d���̍~�������Ȃ��悤�ɐv����Ă���B�o�b�e���[�Ɏg�p�����d���t�͗��_�Ɛ��������������F�E���L�̊_�ŁA����������x�̍������̂��g�p����B�d���t�͐��ɔ̓�_�����A���ɔ̊C�ȏƔ������āA���ꍞ�d����~������A�d�C���������p���s������łȂ��A�Z�������̓d���̓`�����s���B�d���t�̔�d�́A��ʂɊ��S�[�d���ɓd���t���x�Q�O���ɂ�����1.280�}0.010�̂����g�p����Ă���B | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | �@�Ȃ��A�_�i���_�Z�x10%������́j�͓ŕ���������@�Ō����Ɏw�肳��Ă���A���̎戵�ɂ͏\���Ȓ��ӂ��K�v�ł���B�o�b�e���[�p�_�͉��w�I�ɏ����Ȃ��̂łȂ���Ȃ�Ȃ��B���x�̒Ⴂ���̂�p����ƁA���ɔ̕��H��p�𑁂߁A���邢�͎��ȕ��d��傫�����Ď�����Z������B���������āA�ŏ��ɗp����d���t�͂������̂��ƁA�g�p���̓d���t�ɂ��A������s�����̓���ʂ悤���ӂ��Ȃ���Ȃ�Ȃ��B�o�b�e���[�p�_�͓��{�H�ƋK�i�iJIS K 1321�j�ɋK�肳��Ă��鐸���_��p����B�Ȃ��A��߁A�␅�Ȃǂɗp���鐸�����́i�Ёj�d�r�H�Ɖ�K�i�iSBA S0404�j�ŋK�肳�ꂽ�~�d�r�p�������ɂ��B | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
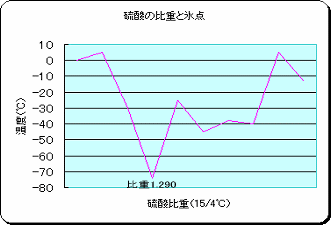
| �@ | �@���x���������ቺ����Ɗ_�͕X�����邪�A���̕X���͗��_�̔�d�ɂ���Ă��ƂȂ�B | |||||||||||||||||||||||||||||||||||||||||||||||||||||||
 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | �@��d��1.290�̂��̂���ԕX�����ɂ����B���̕X���́|�V�T���t�߂ł��邪�A�����荂���Ă��Ⴍ�Ă��X�����₷���Ȃ�A���̕X�_�͍����Ȃ�B�o�b�e���[�̊��S�[�d���̓d���t��d��1.280�i20���j�ł��邩��X�����ɂ������A���d���Ĕ�d��1.100�i20���j���炢�ɒቺ����ƁA���̕X�_�́|�P�O���O��ƂȂ�A�X�����₷���Ȃ�B�d���t�̕X���̓o�b�e���[��j�����邩��A�o�b�e���[����d�����܂ܕ��u���Ȃ��ŁA�K�����S�ɏ[�d���Ă������Ƃ��K�v�ł���B |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@�Q�D�o�b�e���[�̎�ށ@ | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.1�@�o�b�e���[�̌`���Ƃ́E�E�E | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ | �@�i�h�r�iJIS D 5301�@�n���p���~�d�r�j�ɂ��`���̕\���@�ł́A�o�b�e��[�̐��\�Ɛ��@�Ȃǂ��킩��悤�ɂȂ��Ă���B | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| �@ |
�m�`���̈Ӗ��n
�@�@�@�@�@�F�@�T�T�@�̈Ӗ��ˁ@���\�����N �@�@�@�@�A�F�@�c�@�̈Ӗ��ˁ@���w�������̋敪
�@�@�@�@�B�F�@�Q�R�@�̈Ӗ��ˁ@�������@�i�����j�̊T�� �@�@�@�@�C�F�@�k�@�̈Ӗ��ˁ@�[�q�̈ʒu
�h�C�c�c�h�m�K�i�o�b�e���[�̌`���̕\����
�@�@�@�@�F�@�T�@�̈Ӗ��ˁ@�o�b�e���[�̎��
�@�@�@�A�F�@�U�R�@�̈Ӗ��ˁ@�Q�O���ԗ��e�ʂ�\�� �@�@�@�B�F�@�P�W�@�̈Ӗ��ˁ@�o�^�ԍ��@�d�l�̈Ⴂ�ɂ��A�ԂŎ����i�T�C�Y�E�[�q�ʒu�E�r�C�\�����̈Ⴂ�j �č��r�`�d�K�i�o�b�e���[�̌`���̕\���� �@�@�@�č��̃o�b�e���[�̌`���́A�r�`�d�K�i�Ŋ�{�����߂��Ă���A���p�I�ɂ͂����W�J�����`�� �@�@�@�@�@�@�@�r�`�d�Ƃ́@Society of Automotive
Engineers�@�̗��i�č������ԋZ�p�ψ���j |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2.2�@�o�b�e���[�̋����`�Ԃɂ���� | |
| �@ | �@�o�b�e���[�͓d���t�̗L������ыɔ̏�ԂȂǂɂ��A�u�t���[�d�σo�b�e���[�v�A�d���t�𒍓����Ă���g�p����u���p���o�b�e���[�v�̂Q��ނ�����B�t���[�d�σo�b�e���[�́A���ł��g�p�ł���悤�ɁA���[�d���������Ă�����̂ł���B�t���[�d�σo�b�e���[�́A���u���ɕK�����ȕ��d������̂ŁA�e�ʂ��������d���t�̔�d���ቺ����B�܂������̂��߉t�ʂ���������B�]���Ē����ԕ��u�����ꍇ�́A�o�b�e���[���\�������Ȃ�������A�܂��ɔ��������ɉe����^���鋰�ꂪ����̂ŕK������I�Ɂi�Q�`�R�������j�[�d���s���Ďg�p�J�n���邱�Ƃ��]�܂������p���o�b�e���[�͓d���t�𒍓����Ďg�p�ł�����̂ł��邪�A�d���t������ɏ[�d���s���g�p�J�n���邱�Ƃ��]�܂����B���̃o�b�e���[�ł́A���S�[�d��Ԃɂ��鐳�����ɔ����ʂȕ��@�ɂ��_�����Ȃ��悤�Ɋ������đg�ݗ��Ă��A���t���܂ŋɔ��O�C�ɐG��Ď_�����Ȃ��悤�t�������V�[���ȂǂŖ����ꂽ���̂ł���B�]���Ďg�p�J�n�̂��߂ɓd���t�𒍓�����܂ł́A��ɖ������J���Ȃ��悤�ɒ��ӂ��Ȃ���Ȃ�Ȃ��B�g�p�ɍۂ��ẮA�܂��t�������O���Ɠ����ɁA���̔r�C�����̖����i�V�[���Ȃǁj��K���J�����邱�ƁB��������_�́A���̃o�b�e���[�̊��S�[�d���Ɠ�����d�̂��̂Ƃ���B |
| 2.3�@�g�p���̓����@�`�Ԃɂ���� | |
| �@ | �@�o�b�e���[�͋ɔi�q�̂̍�������т���ɉ����Č��܂�����A�`�Ԃɂ�蕪�ނ����B |
| �����ԗp �o�b�e���[ |
�A���`�����o�b�e���[ | |
| �n�C�u���b�h�o�b�e���[ | ||
| �J���V�E���o�b�e���[ | �x���g�`�i�t����t�j | |
| �V�[���`�i����َ��j | ||
| �@ | �@�����ԗp�o�b�e���[�ł́A�A���`�����ܗL�ʂ��ɗ͏��Ȃ�������A�A���`�����̑���ɔ��ʂ̃J���V�E����Y�������������̊i�q���ɔɎg�p����Ă���B�����̋ɔ̑g���킹����ыɔQ�\���ɂ��A���낢��̎�ނ�����B |
| . | �A���`���� �o�b�e���[ |
�n�C�u���b�h �o�b�e���[ |
�J���V�E�� �o�b�e���[ |
|
| �i�q���� �̎�� |
���� | ���|�A���`���� | ���|�A���`���� | ���|�J���V�E�� |
| ���� | ���|�A���`���� | ���|�J���V�E�� | ���|�J���V�E�� | |
| �@�E�A���`�����o�b�e���[ | |
| �@ | �@���ɔA���ɔƂ��ɁA�i�q�ɃA���`�������ܗL�������������g�p����Ă���o�b�e���[�ł���B�i�q�������̃A���`�����͋@�B�I���x�𑝂��Ȃǂ̌��ʂ����锽�ʁA�o�b�e���[�g�p���̌��t�⎩�ȕ��d�̑傫�Ȍ����Ƃ��Ȃ�B�]���āA�g�p���̒���I�ȕ␅�̎��{����ђ������u�̏ꍇ�͒���I�ȏ[�d���K�v |
| �@�E�n�C�u���b�h�o�b�e���[ | |
| �@ | �@���ɔƕ��ɔƂňقȂ鉔�����̊i�q���g�p����Ă���o�b�e���[�̑��̂ł��邪�A���ɔɉ��|�A���`���������i�q�A���ɔɉ��|�J���V�E�������i�q���g�p����Ă���n�C�u���b�h�o�b�e���[����ʓI�ɗp�����Ă���B |
| �@�E�J���V�E���o�b�e���[ | |
| �@ | �@���ɔA���ɔƂ����|�J���V�E�������̊i�q���g�p����Ă���o�b�e���[�ł���B���̃o�b�e���[�́A���ȕ��d����ь��t�������ǍD�ł���B |
| �@�E�V�[���`�o�b�e���[�i����َ��o�b�e���[�j | |
| �@ | �@���̃o�b�e���[�͉��|�J���V�E�������̊i�q���g�p�����������ɔA����Z�p���[�^�[�A�ɔƃZ�p���[�^�����邨�����x�ɒ��������d���t��L���A�V�[���\���Ƃ������̂ł���B���̃o�b�e���[�ł́A�����Ŕ��������K�X���ɔɋz������邽�߁A�����I�Ɏg�p���̓d���t�������Ȃ��A�␅�s�v�ł���B �����ԃo�b�e���[�Ƃ��ẮA�ʏ�̉t���ł���x���g�`�i�t����t�j���嗬�ł��邪�A�ێ炪�o���Ȃ��ꏊ�ɓ��ڂ����Ȃǂ̏ꍇ�ɂ́A���̃V�[���`���g�p����邱�Ƃ������B |
| �@ | |
| �@�R�D�o�b�e���[�̔����@ | |||||||||||||||||||||||||||||||||||||||||
| 3.1�@�o�b�e���[�̉��w���� | |||||||||||||||||||||||||||||||||||||||||
| �@ | �@�o�b�e���[�̕��d���̉��w�ω��́A���Ɋ������̓�_�����iPbO2)�����_���iPbSO4�j�ɕς��A���Ɋ������̊C�ȏi�o���j�����_���iPbsO4�j�ɕς��B�����āA�d���t���̗��_�iH2SO4�j�����iH2O�j�ɂȂ��Ă������߂��߁A�d���t��d�͕��d�ɔ����Ēቺ����B�[�d���̉��w�����́A���̋t�ł���B | ||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||
| 3.2�@�o�b�e���[�̋N�d�� | |||||||||||||||||||||||||||||||||||||||||
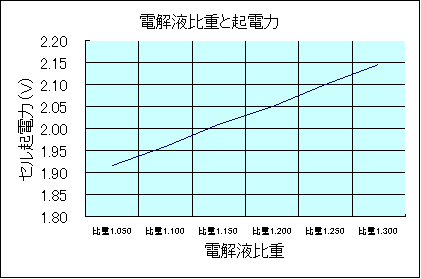
| �@ | �@�o�b�e���[�̋N�d�͂̓Z���i�P�d�r�j�������2.1V�ł���A�d���t�̔�d����щ��x�ɂ���đ����قȂ邪�A�e�ʂ̑傫���ɂ͖��W�ł���B | ||||||||||||||||||||||||||||||||||||||||
| �@ |  |
||||||||||||||||||||||||||||||||||||||||
| 3.3�@���@�d | |||||||||||||||||||||||||||||||||||||||||
| �@ | �@�o�b�e���[����d�C�I�G�l���M�[�����o�����Ƃ���d�Ƃ����A���ɊO���̓d������d�C�I�G�l���M�[�������āA���̏�Ԃɉ����邱�Ƃ��[�d�Ƃ����B�o�b�e���[����d����Ɓi���Ƃ��Γ_�������ꍇ�j�d���t���̗��_�͐��ɔA���ɔ̊������Ɣ������āA���_���ƌĂ�鉻���������B�]���ĕ��d���i�ނɂ�āA���_�̏���ʂ��������A�d���t���̗��_�������Ȃ��Ȃ�A�Z�x���Ⴍ�Ȃ�B�����闰�_�̗ʂ̓o�b�e���[������o���ꂽ�d�C�ʂɐ���Ⴗ��B���_���ɔ̊������Ɣ������ď�����ƃo�b�e���[�d�����~�����āA�d�������o�����Ƃ��ł��Ȃ��Ȃ�B���̂悤�ɕ��d����ɂ�āA�d���t�Z�x���~�����Ă������ۂ𗘗p���Ĕ�d�v���g�p���邱�Ƃɂ��A�o�b�e���[���Ɏc������d�C�ʂ𐄒肷�邱�Ƃ��ł���B |
||||||||||||||||||||||||||||||||||||||||
| 3.4�@�[�@�d | |||||||||||||||||||||||||||||||||||||||||
| �@ | �@���d�����o�b�e���[�ɊO���̓d������A�d���𑗂荞�ނƁA���ɔA���ɔ̗��_������������ė��_�͋ɔ��͂Ȃ�ēd���t���ɖ߂�A���̔Z�x�ɂȂ�B�����ɋɔ̊����������̏�Ԃɖ߂�A�Ăѓd�������o�����Ƃ��ł���悤�ɂȂ�B�[�d���i��Ńo�b�e���[�����S�[�d��Ԃɋ߂Â��ƁA���ɔ��琅�f�K�X�A���ɔ���_�f�K�X����������B�����̃K�X�͔�������L����̂ŁA�o�b�e���[�ɉC���߂Â�����V���[�g��X�p�[�N�������Ă͂Ȃ�Ȃ��B |
||||||||||||||||||||||||||||||||||||||||
| 3.5�@�d���t�Ɣ�d�ω� | |||||||||||||||||||||||||||||||||||||||||
| �@ | �@��d1,280�Ƃ́A���̏d��������1.280�{���邱�Ƃł���B�o�b�e���[����d����Ɠd���t���̗��_���͋ɔ̊������Ɣ������A���_���ƂȂ邽�߂ɁA�d���t�̔�d�͒ቺ����B�d���t�̔�d�͋z����d�v�Ȃǂ��g�p���đ��肷��B�z����d�v�̓S���̈���̂����K���X���Ȃǂ̃X�|�C�g�̒��ɔ�d�ڐ����{�����K���X���̔�d�i�����q�j�������Ă���B�X�|�C�g�œd���t���z���グ��ƁA�t���ɕ��������d�v�i�����q�j�̉t�E�ʂ̖ڐ�����d�������B | ||||||||||||||||||||||||||||||||||||||||
|
|||||||||||||||||||||||||||||||||||||||||
| �@ | �@��}�͔�d�ڐ��̐��������������������̂ŁA�ڂ̈ʒu���X�|�C�g���̉t�ʂƕ��s�ɒu���A�\�ʒ��͂Ő���オ�����t�ʂ̖ڐ���ǂ܂Ȃ���Ȃ�Ȃ��B | ||||||||||||||||||||||||||||||||||||||||
| �@��d�Ə[�d��� | |||||||||||||||||||||||||||||||||||||||||
| �@ | �@�z����d�v�œd���t�̔�d�𑪂�A���̒l�ɂ���ăo�b�e���[�̏[�d��Ԃ𐄑����邱�Ƃ��ł���Əq�ׂ����A���m��������ɂ͓d���t�ʂ��K��̍����ɂȂ��Ă��邱�ƁA�␅�����ꍇ�͏[�d���ēd���t���悭���a���Ă��瑪�肷��K�v������B�\�ɏ[�d��ԂƓd���t��d�i�Q�O���j�Ƃ̊W����ʓI�ȃo�b�e���[�ɂ��ċ��߂����ł���B | ||||||||||||||||||||||||||||||||||||||||
| �@ |
|
||||||||||||||||||||||||||||||||||||||||
| �@���x� | |||||||||||||||||||||||||||||||||||||||||
| �@ | �@��d�v�ő��肵����d�͉��x����Ȃ���Ȃ�Ȃ��B���̔�d�l�͉��x���ς��ƈقȂ����l�������A���x�������ƒႭ�A���x���Ⴂ�ƍ����Ȃ�B����͉��x�������Ɠd���t�e�ʂ��������A�₦��ƌ������邩��ł���B��ʂɃo�b�e���[�̓d���t��d�͉��x�Q�O����W���Ƃ��ėp���A�ω��̊����͉��x�P���̏㏸�ɑ���d��0.0007�ቺ���A���x�P���̍~���ɑ���d��0.0007�㏸����B���鉷�x�ő�������d��W�����x�Q�O���ɂ������d�Ɋ��Z����ɂ́A������p����B | ||||||||||||||||||||||||||||||||||||||||
| �@ |
|
||||||||||||||||||||||||||||||||||||||||
| �@ |
|
||||||||||||||||||||||||||||||||||||||||
| �@ | �@��P�͉Ċ��̏ꍇ�ŁA�����d�l���猩��ƂP�O���ʕ��d������Ԃƍl����ꂽ���A�W�����x�Ɋ��Z����Ǝ��ۂ͊��S�[�d��Ԃɋ߂���ԂƂȂ��Ă���B ��Q�͓~��̏ꍇ�ŁA���肵����d������Ɗ��S�ɏ[�d����Ă���悤�ł��邪�A���ۂ͂X�O�����x�̏[�d��Ԃł���B |
||||||||||||||||||||||||||||||||||||||||
| �@�S�D�o�b�e���[�̏������@ | ||||||||||||||||||||||
| 4.1�@�o�b�e���[�̋K�i | ||||||||||||||||||||||
| �@ | �@�o�b�e���[�̗e�ʁA�������d�A�[�d����A�����Ȃǂ̎������@�́A�i�h�r�K�i�i�i�h�r�@�c�@�T�R�O�P�n���p���~�d�r�j�ɏڍׂɋK�肳��Ă���B�܂��A�֘A����O���̃o�b�e���[�K�i�Ƃ��ĕč��̂r�`�d�K�i�A�h�C�c�̂c�h�m�K�i�Ȃǂ�����B���L�̕\�́A�e�ʁE�������d���\�����̊T�v�ɂ��ċK�i�ʂɎ��������̂ł���B | |||||||||||||||||||||
| �@ |
|
|||||||||||||||||||||
| 4.2�@���d���� | ||||||||||||||||||||||
| �@�o�b�e���[�̗e�ʁ@ | ||||||||||||||||||||||
| �@ | �@�o�b�e���[�̗e�ʂƂ́A���S�[�d���ꂽ�o�b�e���[�̒[�q�d��������̕��d�I�~�d���ɂȂ�܂ŕ��d����ԂɎ��o�����Ƃ̏o����d�C�ʂŌ��߂��Ă���B�o�b�e���[�̗e�ʂ������Ƃ��A���d���܂��͕��d�d��������K�v������B���d���͕��d�d���̑傫�����������̂ŁA�o�b�e���[�̗e�ʂ͎��o���d���̑傫���ɂ���đ傫���ς�邽�߂ł���B | |||||||||||||||||||||
| �@ | �@�i�P�j�@�T���ԗ��e�� | |||||||||||||||||||||
| �@ | �@ | �@���{�̎����ԗp�o�b�e���[�ł͂T���ԗ��e�ʂ��g���Ă���B����͊��S�ɏ[�d�����o�b�e���[��d���t���x�Q�T�}�Q���ɕێ����A�T���ԗ��e�ʂ�1/5�̈��d���i�T���ԗ��d���j�œd����10.5�u�ɍ~������܂ŕ��d�����Ƃ��̗e�ʂł���B | ||||||||||||||||||||
| �@ |
|
|||||||||||||||||||||
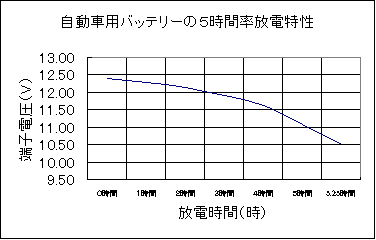
| �@ | �@ | �@���Ƃ��A�P�Q�u�P�Q�O�A���y�A�E�A���[�i�`���j�̃o�b�e���[�͂Q�S�`�i���P�Q�O�`�����T���j�̓d���ŕ��d���A�d����10.5�u�ɍ~������܂ōs���B���̕��d���ԁi���j�ƕ��d�d���i�`���j�̐ς�e�ʁi�`���j�Ə̂��A���̏ꍇ�̗e�ʂ��T���ԗ��e�ʁi�`���^�T�g�q�j�Ƃ����i��i�e�ʂƂ������j���d��ł���d������d�I�~�d���Ƃ����B | ||||||||||||||||||||
| �@ | �@ | �@���}�͂T���ԗ����d�d���ŁA�d����10.5�u�܂ŕ��d�����ꍇ�̓����}�̈��ł���B | ||||||||||||||||||||
| �@ |  |
|||||||||||||||||||||
| �@ | �@�i�Q�j�@���U�[�u�L���p�V�e�B�@�m�q�b�n | |||||||||||||||||||||
| �@ | �@ | �@�T���ԗ��e�ʂ̓o�b�e���[�̕��d�e�ʂ�m�邽�߂ɂ͓K�ȕ��@�ł��邪�A�����Ԃ̏[�d�n�����̏Ⴕ���ꍇ�A�d�C���ׂւ̓o�b�e���[����K�v�ȓd�͂����������B���̂��߂̕K�v�e�ʂ̊�ɂ��Ă̓��U�[�u�L���p�V�e�B�Ƃ����������@�����莟�̕��@�ŕ]������B | ||||||||||||||||||||
| �@ | �@ |
|
||||||||||||||||||||
| �@ | �@ | �@��L�̏����Ńo�b�e���[����d�����ꍇ�A�[�q�d����10.5�u�ɒB���閘�̎��Ԃ𑪒肷��B���̎������Ԃ��i���j�ŕ\�����l�����U�[�u�L���p�V�e�B�Ə̂��Ă���B�����o�b�e���[�̑傫���ɊW�Ȃ��Q�T���łQ�T�`�̈��̓d���ŕ��d�����ꍇ�̕��d���Ԃ��i���j�ŕ\�����̂����U�[�u�L���p�V�e�B�ł���B | ||||||||||||||||||||
| �@���d���Ɨe�� | ||||||||||||||||||||||
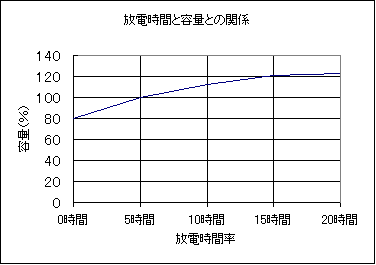
| �@ | �@�o�b�e���[������o������e�ʂ́A���d�d���̑傫���ɂ���ĕω�����B���Ȃ킿���d�d�����傫���قǎ��o����d�C�ʁi�e�ʁj���������A���d�d�����������قǎ��o����d�C�ʁi�e�ʁj���傫���Ȃ�B���̗��R�́A���d�d�����傫���Ȃ�قǓd���t�̊g�U�i���d�̐i�s�ɕ������w�����j���ǂ����Ȃ��Ȃ邽�߂ŁA�ɔ��������E���ł̗��_�̗ʂ��������邽�߂ł���B���}�͕��d���Ɨe�ʂ̊W���������}�ł��� | |||||||||||||||||||||
 |
||||||||||||||||||||||
| �@���x�Ɨe�� | ||||||||||||||||||||||
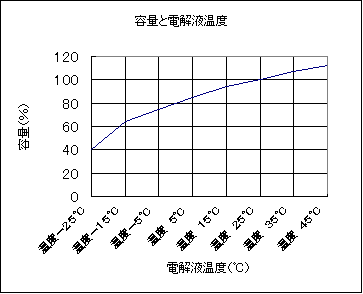
| �@ | �@�o�b�e���[�̗e�ʂ́A�d���t���x�ɂ���đ傫���ω�����B���̕ω��̏�Ԃ́A���}�Ɏ����Ƃ��艷�x��������Ɨe�ʂ͏������Ȃ�B�]���ėe�ʂ�\������Ƃ��́A���̉��x�����Ȃ���Ȃ�Ȃ��B | |||||||||||||||||||||
| �@ | �@�o�b�e���[�̗e�ʂ́A�Q�T������Ƃ���B | |||||||||||||||||||||
 |
||||||||||||||||||||||
| �@�n�����\ | ||||||||||||||||||||||
| �@ | �@�o�b�e���[�̃G���W���n���\�͂́A�G���W�����X�^�[�^�ŁA�n������ۂ̑�d���ɑ�������d���Ńo�b�e���[����d�������Ƃ��A�ǂꂾ���������d�d�����ێ��ł��邩�ɂ���ĕ]�������B�G���W�����n��������Ƃ��Ƀo�b�e���[����X�^�[�^�ɗ����d���́A�G���W���̔r�C�ʁA��]���x�Ȃǂɂ��قȂ邪�A���ʂ̏�p�Ԃł͏퉷�Ŗ�P�O�O�`�R�O�O�`���x�ł���B���͉��x���Ⴍ�Ȃ�ƁA�������̔S�x�������A�n���ɗv����d�����܂���������B | |||||||||||||||||||||
| �@ | �@�i�h�r�K�i�iJIS D 5301�j�ł͒ቷ���̎n�����\�����̍��ڂɋK�肵�Ă���B | |||||||||||||||||||||
| �@ | �i�P�j�@�i�h�r�K�i�ɂ��ቷ�������d���� | |||||||||||||||||||||
| �@ | �@ | �@�@�@�@�E-15���P�T�O�`�A�R�O�O�`�A�܂��͂T�O�O�`�ŕ��d�����ꍇ�A�T�b�ځi�܂��͂R�O�b�ځj�̓d�� �@�@�@�@�E-15���P�T�O�`�A�R�O�O�`�A�܂��͂T�O�O�`�ŕ��d�����ꍇ�A�d�����U�u�ɂȂ�܂ł̕��d�������ԁi���j |
||||||||||||||||||||
| �@ | �i�Q�j�@�R�[���h�N�����L���O�d���i�b�b�`�j | |||||||||||||||||||||
| �č��̂r�`�d�K�i�A�h�C�c�̂c�h�m�K�i�ɂ��ቷ�n�����\ �����ԃo�b�e���[�ł́A�G���W���n���ɕK�v�ȃC�O�j�b�V�����R�C���ւ̓d���A�X�^�[�^�ւ̓d���Ɠd������уG���W���̃N�����L���O���Ԃ��v������Ă���B |
||||||||||||||||||||||
| �@�o�b�e���[�̏�ԁF���S�[�d��� �@���@���@���@�x�@�F�|�P�W���}�P�� |
||||||||||||||||||||||
| �@��L�̏����Œ[�q�d�����R�O�b�ڂ�7,2�u�i�c�h�m�K�i�̏ꍇ��9.0�u�j�ƂȂ�悤�ȕ��d�d�������߂�B���̓d�����R�[���h�N�����L���O�d���Ə̂��Ă���B�Ȃ��A�i�h�r�K�i�ł́A�r�`�d�K�i�ɂ��]���@���Q�l�Ƃ��Ď�����Ă���B | ||||||||||||||||||||||
| �@���ȕ��d | ||||||||||||||||||||||
| �@�o�b�e���[�͓d���t����������ԂŊO����H�ɂȂ��ŕ��d�����Ȃ��Ă��A���Ԃ̌o�߂Ƌ��ɏ��X�ɓd�C�G�l���M�[�������Ă����B���̌��ۂ����ȕ��d�Ƃ����o�b�e���[�̎�ނɂ���Ă��̒l�͈Ⴄ���A�Q�T���łP��������0.1�`0.3���ł���B��ʂɓd���t�̔�d�Z�x����щ��x�������قǁA���w�����Ȃǂɂ�莩�ȕ��d�ʂ͑傫���Ȃ�B | ||||||||||||||||||||||
| �@���}�̓o�b�e���[�̎�ނɂ��A�Q�T���ɂ�������u���ԂƎ��ȕ��d�Ƃ̊W��ł���B | ||||||||||||||||||||||
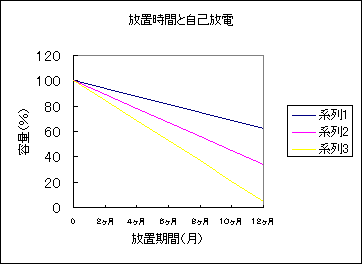 �n��P�F�J���V�E���o�b�e���[ �n��Q�F�n�C�u���b�h�o�b�e���[ �n��R�F�A���`�����o�b�e���[�@ |
||||||||||||||||||||||
| 4.3�@�[�d���� | ||||||||||||||||||||||
| �@ | �@���d�����o�b�e���[���d���[�d�����Ƃ��A�[�q�d���E�d���t��d����щt���Ȃǂ̎��ԂƋ��ɕω�����l�q���[�d�����Ƃ����B | |||||||||||||||||||||
| �@ | �@�i�P�j�[�d���ɂ�����[�q�d���̕ω� | |||||||||||||||||||||
| �@ | �@ | �@�ŏ��͋}�ɏ㏸���A���̌�͊ɂ₩�ɏ㏸�𑱂��A�d������P�S�D�S�u�i�Z���������Q�D�S�u�j�ɒB���鍠����Ăы}���ɏ㏸�A�P�T�`�P�V�u�i�Z���������Q�D�T�`�Q�D�W�u�j�ɒB���Ĉ��l���ێ�����B �@�@���D�[�d�d�����傫���Ɠd���͍����l�������B �@�@���D�d���t���x�������Ɠd���͒Ⴂ�l�������B �@�@���D�d���t��d�������Ɠd���͍����l�������B |
||||||||||||||||||||
| �@ | �@�i�Q�j�[�d���ɂ�����d���t��d�̕ω� | |||||||||||||||||||||
| �@ | �@ | �@�[�d���̔�d�̓K�X�����̎n�܂�܂ł́A�d���t�̝��a���s���Ȃ��̂ŁA���̏㏸�͊ɂ₩�ł��邪�@�K�X�������n�܂�Ƌ}���ɏ㏸���A�[�d�I���ɂ͍ō��l�ɒB���Ă��̌�͈��l���ێ�����B | ||||||||||||||||||||
| �@ | �@�i�R�j�[�d���̃K�X���� | |||||||||||||||||||||
| �@ | �@ | �@�d������P�S�D�S�u�i�Z���������Q�D�S�u�j�ɒB���鍠����K�X����������ɂȂ�A�[�d�I�����߂Â��ɏ]���đ������A���S�[�d��ԂɒB������́A�����d�̖͂w�ǂ����̓d�C�����i�K�X�̔����j�ɏ����邽�ߏ[�d�d���ɑ�������K�X����������B���̂悤�ɃK�X�����̒x���A������Ԃ͏[�d�肷���ŏd�v�Ȃ���łȂ��A�����V���[�g�Ȃǂ̌̏ᔭ���̏d�v�ȃ`�F�b�N�|�C���g�ł���B | ||||||||||||||||||||
| 4.4�@�o�b�e���[�̎��� | ||||||||||||||||||||||
| �@�t����[�d�σo�b�e���[�́A�ۊǁE���u�Ȃǎg��Ȃ��Ă��o�N���A�e�ʂ����X�ɒቺ���������i�s����B�i�h�r�K�i�ł́A�����I���̂Ƃ肩���̊�Ƃ��Ă������̏����̂��Ƃŏ[���d���s���A���̃o�@�b�e���[�̒�i�e�ʂɑ��āA���銄���ȉ��ɒቺ����܂ł̏[���d�i�T�C�N���j�Ŕ��肵�Ă���B�@�������A�����o�b�e���[�ł��g�p�����A�g�p���A�����e�i���X�i����_���j�A�ԗ����̏[�d���u�A��t���ꏊ�Ȃǂ̗v���ɂ���Ď����͈قȂ�̂ŁA�ȒP�Ɍ����Ȃ����A��p�Ԃ̎����ł́A�Q�`�R�N�̂��̂������B | ||||||||||||||||||||||
|
||||||||||||||||||||||
| �@�T�D�o�b�e���[�̏[�d�̂������@ | |
| �@���q�̐���Ȏg�p�����̂��Ƃł́A���s�ɂ���ăo�b�e���[�͏[�d�����ɏ[�d��Ԃɕۂ����悤�v����Ă���B�������A�ԗ����Ԏg�p���Ȃ�������A�o�b�e���[�������ԕ��u���ꂽ��A���C�g�̏����Y��ȂǂŃo�b�e���[�����d���ăG���W���n��������ȏ�ԂɂȂ�B���̂悤�ȏꍇ�ɂ́A�[�d����g�p���o�b�e���[�̏[�d���K�v�ł���B�o�b�e���[�̏[�d�ɂ͒�����ʓd���A�[�d��̓d���A�d���̒������@�ɂ�蕁�ʏ[�d�Ƌ}���[�d�Ƃ�����B | |
| 5.1�@���ʏ[�d | |
| �@�E��d���[�d�@ | |
| �@ | �@�T���ԗ��e�ʂ̂P�^�P�O�̓d���ŏ[�d���s���B |
| �@�E��d���[�d�@ | |
| �@ | �@���̓d�����o�b�e���[�ɗ^���ď[�d������̂ŁA�ԗ��̏[�d�n�i�I���^�l�[�^�ƃ��M�����[�^�j�ɂ��[�d������ɑ������A�d��������d�������ɂȂ��Ă���B�[�d�����ɂ̓o�b�e���[�̕��d��Ԃɉ����Đ������x�̑傫�ȏ[�d�d��������A�[�d�i�s�ɔ����ăo�b�e���[�̒[�q�d�������d���ɒB����ƁA�[�d�d���͌������Đݒ�d���Ɖ��x�����Ɍ������������[�d�d���ƂȂ�B���̏[�d���@�̓K�X�������}�����ēd���t���̐��������N����ɂ����A��r�I�Z���ԂɌ����悭�o�b�e���[���[�d�ł��钷��������B�������A�����ɑ傫�ȏ[�d�d��������邽�߁A����ɉ�������e�ʂ̏[�d�킪�K�v�ł��莩���ԗp����юY�Ɨp�o�b�e���[�Ȃǂɍ̗p����Ă���B�܂��A�K�X�������}�����d���t��d���ψ�ɒ������邽�߁A�K�X�����ɂ��d���t���a�̂��߂ɒ�d���[�d�@�p����K�v������B |
| �@�E����d���[�d�@ | |
| �@ | �@��d���[�d�̕ό`�ŁA��ʂ̏[�d��ł͂��̏[�d�������L���̗p����Ă���B���d���Ă���o�b�e���[�ł́A�����ɑ傫�ȏ[�d�d��������Ē[�q�d�����㏸���A���ꂪ�d���h���b�v�i��R�j�ƂȂ��ăo�b�e���[�ւ̏[�d�d���𐧌䂵�Ă���B�[�d�̐i�s�ɔ����ăo�b�e���[�̒[�q�d�������X�ɏ㏸���A�[�d�d�����������Ă����B |
| �@�E�}���[�d�@ | |
| �@ | �@�[�����d��Ԃɂ���o�b�e���[�����}�I�ɒZ���ԂŃG���W���n���\�Ȓ��x�ɂ��邽�߁A�傫�ȓd���i�T���ԗ��e�ʂ̒l�ȉ��j�ŏ[�d���Ă��̕��d�ʂ̊�������₤���̂��}���[�d�ł���B���̏[�d���@�́A�o�b�e���[�����S�[�d������̂ł͂Ȃ��B�}���[�d�͑�d���ŏ[�d���邽�߁A�d���t���x���㏸����A�K�X�����������A�[�d�������ǂ��Ȃ��Ȃǂ̒Z��������B�]���āA�����ԕ��u���ꂽ�悤�ȃo�b�e���[�̏[�d�ɂ͓K���ł͂Ȃ��B�[�d���Ԃ͂R�O���ȓ��Ƃ��A�d���t���x�͂T�T�����Ȃ��悤�ɂ���K�v������B�������ƃo�b�e���[�����āA�������Z���Ȃ�Ȃǂ̈��e�����o�Ă���B |
| 5.2�@�[�d�̕��@�Ɠ��� | |
| �@�E���[�d | |
| �@ | �@�o�b�e���[�ɓd���t������A�ŏ��ɏ[�d������̂����[�d�Ƃ����B���[�d�͒ʏ탁�[�J�[�ōs���A�t����[�d�σo�b�e���[�Ƃ��Ĕ̔�����Ă���B���p���o�b�e���[�́A�d���t�𒍉t���[�d���Ďg�p������̂ł���B���p���o�b�e���[�ł͕ۊnjo���i�ۊlj��x�A������ԁA�t�����̒��t����ԂȂǁj�ɂ��[�d�ɗv���鎞�Ԃ͑啝�ɕς��A��ʂɕۊNJ��ԂU�����܂ł̏ꍇ�A�K��[�d�d���łR�`�T���Ԓ��x�ł��鑦�p���o�b�e���[�ł͓d���t�������Ă��Ȃ��B�d���t�̒����́A�o�b�e���[�𐅕��ȏꏊ�ɒu���t��������O���A�Y�t���ꂽ�d���t��d�P�D�Q�W�O�i�Q�O���j�̊_���P�Z�����ō��t�ʐ��i�t�o�o�d�q�@�k�d�u�d�k�j�܂��͂ӂ��̉t�����[�̉t�ʎw�����u��[�܂œ����B��������d���t�̉��x�́A�P�T�`�R�T���͈̔͂Ƃ��邱�ƁB��R�O���o�߂���Ɖt�ʂ��ቺ����̂ŁA�ēx�d���t���[���ď[�d���s���B |
| �@�E�[�d�i�[�d�j | |
| �@ | �@�ԗ��̃��C�g�̏����Y��Ȃǂɂ����d��o�b�e���[�̒������u�i�ԗ��̒����s�g�p���܂ށj�ɂ�鎩�ȕ��d�ŗe�ʂ��������ꍇ�ɂ́A�G���W���n��������ɂȂ�B�[�d�i�[�d�j�̓o�b�e���[�̗e�ʂ������邽�߂ɍs�����̂ł���B |
| 5.3�@�[�d��̎戵 | |
| �@�i�P�j�[�d��̑I�ѕ� | |
| �@ | �@�E�[�d����o�b�e���[�̌��̓d���Ɠ����d���̏[�d���I�Ԃ��ƁB�[�d��ɐؑփX�C�b�`������ꍇ�ɂ́A�d���ݒ���s���B�Q�̃o�b�e���[���ɏ[�d����ꍇ�́A�Q�S�u�p�̏[�d����g�p���Ē���ɐڑ����邱�ƁB |
| �@�i�Q�j�[�d��ƃo�b�e���[�Ƃ̐ڑ��菇 | |
| �@ | �@�E�[�d��̓d���Ɠd�������c�}�~���n�e�e�i�j�ɂȂĂ��邱�Ƃ��m�F���A�[�d��̃R�[�h���R���Z���g�ɍ������� �@�E�v���X�[�d�N���b�v���o�b�e���[�̃v���X�[�q�ɁA���Ƀ}�C�i�X�[�d�N���b�v���o�b�e���[�̃}�C�i�X�[�q�ɂ�������Œ肷�邱�ƁB�t�ɐڑ�����ƁA�@�푹����o�b�e���[�����̌����ƂȂ�B �@�E�[�d��̓d�����n�m�i���j�ɂ��A���ɓd�������c�}�~���ď[�d�d��������B�[�d�I����͓d�������c�}�~���n�e�e�i�j�ɂ��A���ɏ[�d��̓d�����n�e�e�i�j�ɂ���B |
| �@�i�R�j�[�d�d���Ə[�d���x�̊Ǘ� | |
| �@ | �@�E�[�d�d���̓o�b�e���[�̗v���\�̕��ʏ[�d�d���ȉ��̒l�ɁA�}���[�d�ł̓o�b�e���[�̂T���ԗ��e�ʂ̒l�ȉ��łR�O���ȓ��ɐݒ肷�邱�ƁB �@�E�[�d���ɓd�t���x���S�T������ꍇ�́A�[�d�d���������邩�[�d���ꎞ��~���邱�ƁB�}���[�d�̏ꍇ�A�d���t���x���T�T�����鎞�ɓ��l�ȏ��u���s���B |
| �@�i�S�j�[�d�����̂߂₷ | |
| �@ | �@�E�o�b�e���[�̊e�Z�����炳����ɃK�X���������A�[�d���̒[�q�d�����P�T�D�OV�ȏ�A�܂��͓d���t��d���P�D�Q�V�O�i�Q�O���j�ȏ�ɂȂ��Ă����Ԃ������B |
| �@�i�T�j�[�d��̃o�b�e���[�_�� | |
| �@ | �@�E�d���t�ʂ��ō��t�ʐ��i�t�o�o�d�q�@�k�d�u�d�k�j�ɂ��邱�Ƃ��m�F���A�t�������ɂ݂��Ȃ��悤�ɂ�������ƒ��t���邱�ƁB�o�b�e���[�̊O�ς�����Ă���ꍇ�ɂ́A�����邩�������z�Ő��|����B |
| �@�i�U�j�[�d���̈��S�戵�� | |
| �@ | �@�E�[�d��̎戵���������n�ǂ��邱�ƁB�戵�����ƁA�o�b�e���[�̈��Δ����̌����ƂȂ�B �@�E�o�b�e���[���[�d����Ɛ��f�K�X����������̂ŁA�C���߂Â������ʂ��̗ǂ��ꏊ�ōs�����ƁB �@�E�[�d��̓d�����n�m�i���j�̏�Ԃŏ[�d�N���b�v���o�b�e���[�ɐڑ�������A�[�d���ɏ[�d�N���b�v�̎�O�������Ȃ����ƁB�X�p�[�N�ɂ�蔚���̌����ƂȂ�B �@�E�d���t�ʂ��Œ�t�ʐ��i�k�n�v�d�q�@�k�d�u�d�k�j�ȉ��ɒቺ������Ԃŏ[�d������ƃo�b�e���[�����̌����ƂȂ�B�]���āA�d���t�ʂ��t�ʐ��Ԃ̔����ȉ��ɒቺ���Ă���ꍇ�́A�[�d�O�ɐ��������ō��t�ʐ��i�t�o�o�d�q�@�k�d�u�d�k�j�܂ŕ�[���A�ō��t�ʁi�t�o�o�d�q�@�k�d�u�d�k�j�ȏ�ɓ���Ȃ����ƁB�t����̌����ƂȂ�B �@�E�[�d���ɂ̓o�b�e���[�̉t�������O������͎̂�O���A��������K�X���g�U���₷���悤�ɂ��邱�ƁB�t�����ɂ͓d���t���t�����Ă���̂ŁA�畆��ߕ��ɕt���Ȃ����ƁB �@�E�[�d����̃o�b�e���[�́A�R�O���ȓ��ɂ͎ԗ��Ɏ�t���Ȃ����ƁB �@�E��ނ��ԗ��ɓ��ڂ����܂܂ŏ[�d����ꍇ�́A�o�b�e���[�ɐڑ�����Ă���ԗ����̃}�C�i�X�P�[�u���[�q����O�����ƁB |
| �@�@ | |
| ���L�́w�o�b�e���[�̒m���x�ɂ��Ă͎Вc�@�l�E�d�r�H�Ɖ�̎�������\���������̂ł��B ���Вc�@�l�E�d�r�H�Ɖ�ւ̃����N�� |